Huk propagandowy a fakty o MONKEYPOX (mPOX)
Mało znana firma z Danii, która na rynku ma tylko pięć produktów otrzymała zamówienia na szczepionki na tzw. “małpią ospę (mPOX). W zależności od procesu marketingowego my, w Europie, możemy również spodziewać się, że EMA (European Medicines Agency) otrzyma od swojego starszego brata zamówienia dotyczące liczby „szczepionek”, w które musimy zaopatrzyć się w odpowiednim czasie. Współczynnik przeżycia zakażenia ospą małpią (mPOX) na całym świecie wynosi 99,942%. Spośród 80 850 przypadków małpiej ospy udokumentowanych od 2022 r. tylko 55 zakończyło się zgonem. Nie zidentyfikowano żadnych chorób współistniejących ani możliwych czynników społeczno-ekonomicznych. Globalne wskaźniki rozpowszechnienia w 2024 r.
Globalne wskaźniki rozpowszechnienia w 2024 r.
W 2024 r. najwyższa liczba zgłoszonych infekcji na świecie wyniosła 64. Najnowsze statystyki z drugiej połowy lipca pokazują, że światowy wskaźnik chorobowości wynosi od 3 do 8 przypadków dziennie. Tak jest wszędzie na świecie. Nie dotyczy to tylko USA, Wielkiej Brytanii, Australii czy Kanady. To dotyczy całego świata. Rząd Stanów Zjednoczonych wydał już 157 milionów dolarów na zakup szczepionek przeciwko ospie małpiej JYNNEOS od mało znanej firmy farmaceutycznej z siedzibą w Danii: “Bayernian Nordic”. Firmy, która produkuje tylko pięć produktów. Można śmiało założyć, że niesprawdzona szczepionka zostanie ponownie wykorzystana.
Serca zwykłych akcjonariuszy, takich jak Fundacja Gates & Melinda Gates Foundation, będą mogły bić szybciej, proporcjonalnie do wzrostu cen, podczas gdy rozszerzona zgoda zostanie przeforsowana pro forma w przyszłym tygodniu.
Raport EuroBiotech — Bavarian Nordic, Nabriva, Immunocore, Glythera-Iontas i Sanofi
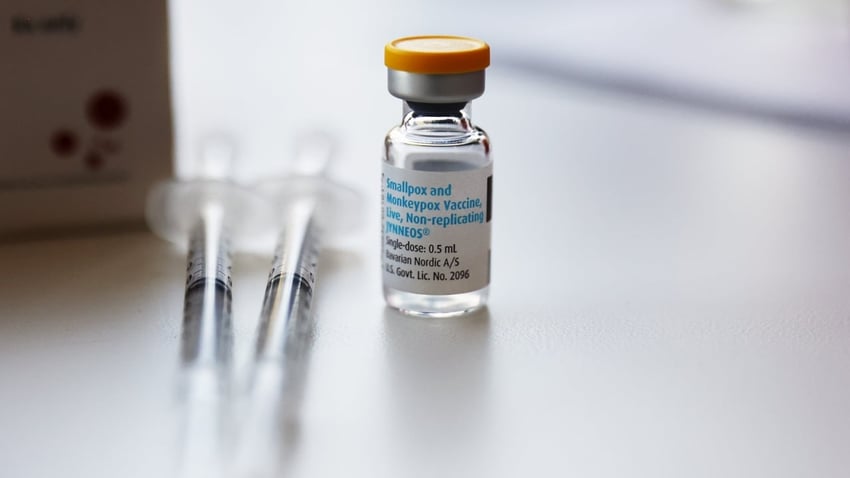
Bavarian Nordic zdobywa kontrakt o wartości 157 mln dolarów na uzupełnienie zapasów szczepionki przeciwko ospie prawdziwej/mpox w USA Jynneos.
Po wprowadzeniu na rynek szczepionki przeciwko ospie prawdziwej/MPox firmy Bavarian Nordic na początku tego roku, duńska firma podpisała kolejną umowę na dostawy z rządem USA.
Urząd ds. Zaawansowanych Badań i Rozwoju Biomedycznego (BARDA) przekazał Bawarskim Krajom Nordyckim 156,8 mln dolarów na „częściowe uzupełnienie” zapasów szczepionek w odpowiedzi na wybuch epidemii MPox, choroby znanej wcześniej jako ospa małpia, w 2022 r.
Wcześniej BARDA miała swój udział w opracowaniu liofilizowanej wersji szczepionki, która w 2019 r. uzyskała pierwszą zgodę FDA.
Umowa o uzupełnieniu zapasów jest konieczna, aby wypełnić obowiązującą umowę firmy Bavarian Nordic ze Stanami Zjednoczonymi, dotyczącą dostarczania liofilizowanej wersji szczepionki nowej generacji służącej do ochrony przed ospą prawdziwą, wyjaśniła firma w komunikacie prasowym.
Bavarian Nordic ma otrzymać 139,7 mln USD za sam produkt szczepionkowy, który zostanie wyprodukowany i zafakturowany w 2024 r. Pozostałe 17 mln USD objęte umową pomoże w finansowaniu dodatkowych usług w latach 2025–2027, w tym magazynowania dawek szczepionki w USA, poinformował Bavarian Nordic.
Transakcja nie podniesie ogólnych wytycznych finansowych Bavarian Nordic na 2024 r., ale zwiększy wartość zabezpieczonych kontraktów w działalności publicznej firmy w tym roku. Ogólnie rzecz biorąc, Bavarian Nordic spodziewa się, że jego działalność publiczna w zakresie gotowości wygeneruje od 2,7 mld koron (395 mln USD) do 3 mld koron (439 mln USD) w 2024 r.
Bavarian Nordic spodziewa się, że w całym roku 2024 sprzedaż wyniesie od 5 miliardów koron (731 milionów dolarów) do 5,3 miliardów koron (775 milionów dolarów) dzięki dodatkowym przychodom ze sprzedaży szczepionek dla podróżnych i produkcji kontraktowej.
Prawie rok temu Bavarian Nordic podpisało pierwszą umowę z USA na uzupełnienie zapasów sprzętu Jynneos o wartości 120 milionów dolarów.
Najnowsza umowa uzupełnienia zapasów pojawia się kilka miesięcy po tym, jak firma wprowadziła Jynneos na rynek komercyjny w USA. Zainteresowane osoby mogą teraz uzyskać dostęp do zastrzyku w lokalnych aptekach i gabinetach lekarskich, a także w niewielkiej grupie klinik wyznaczonych przez władze ds. zdrowia.
Wprowadzenie szczepionki na rynek nastąpiło po decyzji z października 2023 r. Doradczego Komitetu ds. Praktyk Szczepień przy amerykańskich CDC, który zalecił szczepienie szczepionką Jynneos jako rutynową szczepionką dla dorosłych narażonych na zakażenie MPox.
Chociaż mpox nie jest już uważany za nagły przypadek medyczny, jak w 2022 r., w USA co miesiąc pojawia się około 200 przypadków. W kwietniu w USA zgłoszono ponad 32 000 przypadków mpox od wybuchu epidemii w 2022 r.
Szczepionki przeciwko ospie małpiej (Mpox) i ich skutki uboczne: druga strona medalu
Na progu eradykacji ospy prawdziwej, małpia ospa ludzka (Mpox) – zgodnie z zaleceniami WHO (“Kto rekomendował nową nazwę na zarazę Mbox“) – została odkryta w Demokratycznej Republice Konga (DRK) w roku 1970, kiedy sporadyczne przypadki zgłoszono na obszarach wiejskich DRK. Jest to zoonoza bez zidentyfikowanego ostatecznego żywiciela rezerwuarowego. Poza DRK zgłaszano ją w sąsiednich krajach Afryki Zachodniej i Środkowej, w tym w Nigerii, Kamerunie, Sierra Leone, Republice Konga i Liberii . Przez dziesięciolecia wirus był ograniczony tylko do tej części świata, chyba że od początku maja 2022 r. zaczęto zgłaszać ogniska choroby w różnych krajach nieendemicznych. Liczba przypadków wzrosła globalnie tak bardzo, że WHO ogłosiła tę wielokrajową epidemię jako stan nadzwyczajny zdrowia publicznego o zasięgu międzynarodowym 23 lipca 2022 r. Na dzień 23 listopada 2022 r. łączna liczba potwierdzonych przypadków Mpox wynosi 80 850, z czego 55 zgonów dotyczyło 110 krajów, z czego 103 to kraje nieendemiczne.
Wirus Mpox należy do rodziny Poxviridae , rodzaju Orthopoxvirus , który jest podobny do wirusa ospy prawdziwej. Dlatego szczepionki przeciwko ospie prawdziwej mogą zapewniać ochronę również przed Mpox ze względu na reaktywność krzyżową.
Mpox ma dwa warianty (I: wariant środkowoafrykański; II: wariant zachodnioafrykański), z których wariant II jest odpowiedzialny głównie za obecne ogniska choroby. Ta przerażająca sytuacja niemal skłania się ku nowej pandemii, co można w znacznym stopniu powiązać z zanikającą odpornością na Orthopoxvirus , szczególnie u młodszej populacji, która nie jest na nią odporna, z powodu zaprzestania szczepień przeciwko ospie prawdziwej. Mimo że choroba ustępuje samoistnie u większości pacjentów, istnieje stałe zagrożenie braku specyficznego leczenia i wysoki wskaźnik wtórny wynoszący 9,28% u osób niezaszczepionych.
W związku z tym, aby ograniczyć liczbę zachorowań, WHO dokonała przeglądu strategii szczepień przeciwko ospie prawdziwej w 2013 r., aby do szczepień przeciwko Mpox stosować dostępne szczepionki przeciwko ospie prawdziwej. Przegląd przeprowadzono 24 czerwca 2022 r., a następnie 24 sierpnia 2022 roku.
Obecnie dostępne są trzy opcje (ACAM2000, MVA-BN, LC-16) szczepień przeciwko Mpox, z których ACAM2000 jest szczepionką drugiej generacji, a MVA-BN i LC-16 są szczepionkami trzeciej generacji przeciwko ospie. Wszystkie trzy szczepionki są zatwierdzone do stosowania przeciwko Mpox przez różne jurysdykcje, ale ich dostępność różni się w zależności od obszaru geograficznego. Spośród trzech szczepionek MVA-BN, popularnie znana jako JYNNEOS (inne nazwy marek – Imvamune i Imvanex), jest zatwierdzona przez amerykańską Agencję ds. Żywności i Leków (FDA) do zapobiegania zarówno ospie prawdziwej, jak i ospie małpiej i jest główną szczepionką stosowaną przeciwko Mpox w Stanach Zjednoczonych. Jednak ACAM2000 jest zatwierdzona przez amerykańską Agencję ds. Żywności i Leków (FDA) przeciwko ospie prawdziwej i dostępna do stosowania w szczepieniach przeciwko Mpox w ramach protokołu Expanded Access Investigational New Drug (EA-IND) sponsorowanego przez Centra Kontroli i Zapobiegania Chorobom
JYNNEOS (BARDA, Bioshield) to jedyna szczepionka obecnie zatwierdzona (od 2019 r.) przeciwko Mpox. Jest to replikacyjnie niedoborowa szczepionka z żywym wirusem zawierająca osłabiony (niereplikujący) wirus Orthopoxvirus – Modified Vaccinia Ankara-Bavarian Nordic (MVA-BN). Jest zatwierdzona do stosowania u osób powyżej 18 roku życia, dwie dawki po 0,5 ml drogą podskórną, w odstępie 4 tygodni. Jednak 9 sierpnia 2022 r. amerykańska Agencja ds. Żywności i Leków (FDA) zezwoliła na podawanie szczepionki drogą śródskórną populacji wysokiego ryzyka w wieku co najmniej 18 lat, co wymaga mniejszej ilości (jednej piątej, 0,1 ml) dawki szczepionki, aby zwiększyć zasięg szczepień. Jednak w przypadku młodszych osób (<18 lat) zalecaną drogą pozostała podskórna. Decyzja ta została podjęta na podstawie wyników badania klinicznego przeprowadzonego przez Frey i in . w roku 2015, w którym wykazano, że podanie śródskórne wywołało taką samą odpowiedź immunologiczną, ale przy mniejszej ilości szczepionki niż w przypadku podania podskórnego.
Szczepionka została pierwotnie opracowana w celu zwalczania wszelkich prawdopodobnych ataków bioterrorystycznych ospy prawdziwej u osób z obniżoną odpornością jako alternatywa dla starszej szczepionki ACAM2000. Później została zatwierdzona do stosowania w obszarach endemicznych u osób wysokiego ryzyka w celu zwalczania Mpox.
ACAM2000 (Acambis, Canton, Massachusetts) to replikująca się żywa szczepionka przeciw wirusowi ospy, uzyskana przez oczyszczanie płytki z wcześniej dopuszczonej szczepionki produkowanej przez limfę cielęcą – Dryvax (Wyeth Pharmaceutical Inc, Philadelphia, Pennsylvania) i dodatkowo pasażowana trzy razy w liniach komórkowych Vero. Jest uważana za replikującą się szczepionkę przeciw ospie drugiej generacji, zatwierdzoną do stosowania przez US FDA od 2007 r.
Ta szczepionka nie jest zatwierdzona do leczenia Mpox, ale może być stosowana w tym samym celu zgodnie z mechanizmem EA-IND amerykańskiej Agencji ds. Żywności i Leków (FDA), który wymaga świadomej zgody wraz z dodatkowymi wymogami IND. Ta szczepionka jest podawana w pojedynczej dawce, przezskórnie, przy użyciu techniki rozwidlonej igły – wielokrotnych nakłuć (skaryfikacja) 9 . Jedna dawka szczepionki ACAM2000 zawiera stężenie wirusa w zakresie od 1,0 do 5,0×108 jednostek tworzących płytkę (PFU)/ml lub 2,5–12,5×105 PFU /dawkę, a także 2% albuminy USP i śladowe ilości neomycyny i polimyksyny B.
LC-16 (KM Biologics, Japonia) to atenuowany, częściowo replikujący szczep Lister wirusa ospy. Jest podawany w pojedynczej dawce, jako ACAM2000, metodą rozdwojonej igły i skaryfikacji. Jest to szczepionka przeciw ospie prawdziwej trzeciej generacji.
Skutki uboczne szczepionki ACAM2000
Wiadomo, że szczepionka ACAM200 powoduje działania niepożądane, takie jak ból w miejscu wstrzyknięcia, ból węzłów chłonnych, świąd i inne objawy grypopodobne. Inne częste działania niepożądane to – swędzenie, bóle mięśni, ból głowy, ból ramienia, wysypka, gorączka i zmęczenie (https://www.fda.gov/media/75792/download). Otrzymanie tej szczepionki nie jest takie samo jak otrzymanie pojedynczego zastrzyku; wymaga wykonania 15 małych nakłuć skóry za pomocą rozwidlonej igły. Miejsce szczepienia należy pielęgnować, aż strup odpadnie; w przeciwnym razie istnieje potencjalne ryzyko rozprzestrzeniania się żywego wirusa z miejsca szczepienia na inne części ciała lub na inne osoby. Strup zwykle odpada po 2–4 tygodniach, więc do tego czasu zaszczepiona osoba staje się potencjalnym źródłem rozprzestrzeniania się infekcji, szczególnie wśród osób z obniżoną odpornością. Przypadkowa oczna oskrzelowa może wystąpić u niektórych narażonych osób, powodując takie objawy jak – bolesne łzawienie oczu z niewyraźnym widzeniem, bliznowacenie rogówki, zapalenie rogówki i ślepota (https://www.fda.gov/media/75792/download).
Zgłaszano, że ciężkie i długotrwałe skutki uboczne, takie jak zapalenie mięśnia sercowego i osierdzia, występują u około 20 osób na 100 000 osób zaszczepionych szczepionką ACAM2000. Zdarzenia neurologiczne zgłoszono u około dwóch osób na 100 000 osób zaszczepionych szczepionką ACAM2000. Według US FDA, częstość występowania zapalenia mięśnia sercowego/zapalenia osierdzia wynosi 1 na 175 nowych osób zaszczepionych szczepionką ACAM2000. Niewiele badań klinicznych wykazało, że częstość występowania zapalenia mięśnia sercowego i osierdzia wynosi 5,7 na 1000 nowych szczepionek bez żadnej możliwej do zidentyfikowania przyczyny. Niektóre z poważnych, ale rzadkich, długoterminowych skutków ubocznych to – zakażony pęcherz w miejscu szczepienia, ciężka reakcja alergiczna (eczema vaccinatum), rozsiane zakażenie innych części ciała (postępująca ospy krowiej), zapalenie mózgu, zapalenie mózgu i rdzenia kręgowego oraz encefalopatia, a nawet śmierć. Czynnikami ryzyka poważnych skutków ubocznych mogą być – choroby skóry/alergie, choroby serca, stany obniżonej odporności, palenie, wysokie ciśnienie krwi, wysoki poziom cukru we krwi/cholesterolu, ciąża, laktacja, stosowanie kropli do oczu ze sterydami itp. Istnieje ryzyko urodzenia martwego dziecka lub śmierci płodu z powodu szczepienia ACAM2000 u kobiet w ciąży (https://www.fda.gov/media/75792/download).
Ponadto ryzyko przypadkowego zaszczepienia niemowląt żywym wirusem ospy krowiej ACAM2000 od matek karmiących piersią jest poważnym problemem. Osoby uczulone na neomycynę i polimyksynę B są narażone na zwiększone ryzyko ze względu na obecność tych antybiotyków w preparacie ACAM2000.
Skutki uboczne szczepionki MVA-BN
Do tej pory JYNNEOS wydaje się być bezpieczniejszą opcją, aby zdecydować się na szczepienie przeciwko Mpox, które zostało należycie zatwierdzone również w tym celu. Jednak badania muszą zostać jeszcze przeprowadzone, aby poznać pełny profil bezpieczeństwa i immunogenność szczepionki. Jednak stwierdzono, że jest ona bezpieczna dla pacjentów z obniżoną odpornością, takich jak biorcy przeszczepów, pacjenci z HIV i atopowym zapaleniem skóry. W różnych badaniach klinicznych miejsca wstrzyknięcia szczepionki zgłaszano reakcje takie jak zaczerwienienie, stwardnienie/napięcie, ból, stwardnienie, swędzenie, ból gardła, bóle mięśni, ból głowy, dreszcze i nudności, które są możliwe do opanowania i mniej poważne niż działania niepożądane szczepionki ACAM2000.
Raport autorstwa Rao i in. stanów, zgodnie z zaleceniami Advisory Committee on Immunization Practices – USA, istnieje niewielka pewność co do faktu, że JYNNEOS powoduje mniej poważnych zdarzeń niepożądanych niż ACAM2000, po przeanalizowaniu trzech randomizowanych badań kontrolowanych i 15 badań obserwacyjnych, obejmujących łącznie 5775 osób. Niedawne retrospektywne badanie kohortowe przeprowadzone przez Sharff i in . udokumentowało 10 przypadków zdarzeń sercowych występujących po podaniu szczepionki JYNNEOS w okresie od lipca do października 2022 r. w kohorcie populacji północno-zachodnich Stanów Zjednoczonych (Oregon). Jednak bezpośredniego związku tych zdarzeń ze szczepionką nie można było w pełni ocenić20 . WHO stwierdza, że lokalne zdarzenia niepożądane były często zgłaszane w przypadku szczepionek MVA-BN (do 99%). Jednak nie odnotowano przypadków poważnych zdarzeń niepożądanych, takich jak zapalenie mięśnia sercowego lub konieczność hospitalizacji wśród 9713 szczepionek MVA-BN z 19 badań klinicznych. Ze względu na dowody wskazujące na mniejsze skutki uboczne, Doradczy Komitet ds. Praktyk Szczepień zalecił 3 listopada 2021 r. stosowanie szczepionki JYNNEOS jako zamiennika szczepionki ACAM2000 w celu uodpornienia osób narażonych na zakażenie wirusem Orthopoxvirus.
Skutki uboczne szczepionki LC16m8
Łagodne do umiarkowanych miejscowe i ogólnoustrojowe działania niepożądane są bardzo częste w przypadku tej szczepionki. Jednak poważne działania niepożądane, takie jak zapalenie mózgu i objawowe zapalenie mięśnia sercowego, nie zostały zgłoszone w badaniach klinicznych i badaniach kohortowych. Szczepionka nie jest zalecana do powszechnego szczepienia wśród pacjentów z obniżoną odpornością i atopowym zapaleniem skóry, chociaż dowody przedkliniczne potwierdzają zasadność stosowania szczepionki LC16m8 u tych osób.
Wnioski:
Obecnie masowe szczepienia populacji przeciwko Mpox nie są uzasadnione, ponieważ nie wszyscy ludzie są narażeni na zwiększone ryzyko zachorowania. Profilaktyka przedekspozycyjna jest zalecana w przypadku bliskiego kontaktu i populacji wysokiego ryzyka, takich jak dzieci, pacjenci z obniżoną odpornością, mężczyźni uprawiający seks z mężczyznami – populacja homoseksualna, osoby mające wielu niezabezpieczonych partnerów seksualnych, pracownicy służby zdrowia i pracownicy laboratoriów pracujący z Mpox. Profilaktyka poekspozycyjna jest zalecana w przypadku bliskiego kontaktu z osobami zarażonymi w ciągu 4 dni od kontaktu. W przypadku kobiet w ciąży i karmiących piersią oraz dzieci należy podawać niereplikujące szczepionki MVA-BN.
Chociaż w celu kontrolowania ognisk Mpox, szczepienie jest kluczem, przed szczepieniem należy rozważyć kilka kluczowych punktów dotyczących stosunku ryzyka do korzyści oraz bezpieczeństwa i dokładności szczepionki. Nie mamy badań, aby wyciągnąć jednoznaczne wnioski na temat wyżej wymienionych aspektów, dla których oczekujemy wyników i danych z dalszych badań nad dostępnymi szczepionkami Mpox.
Ulotka dołączona do opakowania JYNNEOS 1
Źródła:
- “Raport EuroBiotech — Bavarian Nordic, Nabriva, Immunocore, Glythera-Iontas i Sanofi” – Fiercebiotech 2017-09-21
- “Bavarian Nordic zdobywa kontrakt o wartości 157 mln dolarów na uzupełnienie zapasów szczepionki przeciwko ospie prawdziwej/mpox w USA Jynneos” – Fiercebiotech 2024-08-08
- “Szczepionki przeciwko ospie małpiej (Mpox) i ich skutki uboczne: druga strona medalu” – National Institutes of Health 2023-02-16
- “Ulotka dołączona do opakowania JYNNEOS” – FDA (Food and Drug Administration)